日韩欧美防疫物资需求剧增,口罩出口指南,看这篇就够了
导读:截止今日,全球新冠肺炎病例已超过1100万,数据还在不断上升,各国对口罩的需求也急剧增加,中国作为口罩生产大国,也在抗疫中为各国进行了援助和支持。仅两个月,中国验放出口口罩达278亿,我国口罩日产1个月翻13倍!

国内口罩需求已经平稳,国外急缺,那么出口口罩都需要准备什么,出口申报流程又是如何呢?驼驮小编这就来带你了解。
出口通关流程:
报关前提条件收发货人注册编码(慈善机构可为临时编码),需办理无纸化通关法人卡。
出口资质口罩出口生产销售单位、境内发货人,需满足国内生产、市场流通资质需求。
出口申报要求:
商品归类:除特殊情况外,绝大部分口罩应归入税号63079000;
检验检疫:口罩为非法检产品,申报时检验检疫项目无需填报;特别注意:对出口伊朗等少数几个国家的产品需按规定进行装运前检验。
关税征免:贸易出口:征免性质为申报一般征税,征免方式为申报照章征税;捐赠性质:境内发货人为贸易代理商、慈善机构等,征免性质可不填,征免方式申报全免;
禁限管理:目前商务部未对口罩设置贸易管制要求,中国海关也无针对防护物资的监管证件口岸验核要求;
申报规范:按照规范申报要求填写商品名称、成分含量;如物资非中国生产,原产国按照实际生产国填写。
出口退税口罩的出口退税率为13%
中美关税排除加征美国贸易代表处表示:对从中国进口的口罩等部分医疗产品取消加征关税。
快速通关保障物资出口申报如遇单窗等系统故障,可联系现场海关采取应急方式处置,或者拨打海关12360热线。
口罩出口需要的资质信息:
1.营业执照
2.企业生产许可证
3.产品检验报告
4.医疗器械注册证(非医用不需要)
5.产品说明书、标签
6.产品批次/号
7.产品质量安全书或合格证
8.产品样品图片及外包装图片
9.贸易公司须取得海关收发货人注册备案
出口医疗物资的企业需要什么资质?
对于普通口罩等非医疗器械的物资,没有监管条件,有进出口权许可证即可。涉证的口罩等疫情物资,需要产品三证:
营业执照(经营范围包含有医疗器械相关)
产品备案证或者注册证
厂家检测报告注:如果企业想赠送或代海外关联公司采购,需要提供情况说明。某些贸易公司没有医疗器械的资质,只要厂家提供三证也是可以出口的。
值得特别注意的是,出口伊朗是比较复杂的,需要在伊朗申请COI认证,中文为符合性核查,是伊朗进口强制发件要求的相关检查。
国外口罩出口需要的资质信息:首先要提醒的是,不论是个人还是企业邮寄/出口口罩,都需要保证口罩是合格产品。
这可以在国家药监局查询:登录“国家药品监督管理局”官网,点击“医疗器械-国产器械”的栏目。输入该款口罩的医疗器械注册证号或企业名称等,就可以知道与产品相关的企业生产信息,批准文号信息,即可了解是否为合格产品。
如个人邮寄口罩到美国,可以考虑FEDEX、UPS、DHL、EMS、SF等快递公司。DHL会要求寄件人提供美国的FDA认证,也有的DHL、FEDEX拒收。

各国对口罩出口相关要求
韩国
必要资料:提单,箱单,发票,韩国进口商营业执照准入门槛:韩国医疗器械基本分类为I、II、III、IV类,持证为韩国公司(License holder),韩国收货人需要到韩国药监局Korea Pharmaceutical Traders Association. 提前备案进口资质。注企业自用又是受赠的情况,可以自行进口,不需要有相关资质。口罩要求:口罩还需要有详细的原产地标识,如果是中国制造务必有标签:Made in China, 生产厂家信息,保质期,还要准备成分含量说明,制造工艺流程等,货物到了韩国以后还需进行精简化验送交样品到实验室,化验合格后方可进入韩国市场销售流通。
日本
必要资料:提单,箱单,发票出口日本的PMDA注册医疗器械公司想把产品投放到日本,必须要满足日本的Pharmaceutical and Medical Device Act (PMD Act),在PMD Act的要求下,TOROKU注册系统要求国外的制造商必须向PMDA注册制造商信息。口罩包装要求:包装上印有病毒拦截99%的字样PFE:0.1um微粒子颗粒过滤效率BFE:细菌过滤率VFE:病毒过滤率
美国
必要资料:提单,箱单,发票注册许可证:美国FDA注册许可准入门槛(下方延伸阅读有详解):必须取得美国 NIOSH检测认证,即National Institute for Occupational Safety and Health美国国家职业安全卫生研究所认证。口罩要求:根据HHS(美国卫生及公共服务部)法规,NIOSH(美国国家职业安全卫生研究所)将其认证的防颗粒物口罩分为9类。具体的认证则由NIOSH下属的NPPTL 实验室操作。要注意的是,N95不是特定的产品名称,只要符合N95标准,并且通过NIOSH审查的产品就可以称为“N95型口罩”。
欧盟
必要资料:提单,箱单,发票准入门槛:必须须获得CE认证证书。CE认证是欧盟实行的强制性产品安全认证制度,目的是为了保障欧盟国家人民的生命财产安全。口罩要求:在欧盟口罩属于PPE个人防护用品,医用口罩对应的欧盟标准是EN14683。
澳大利亚
必要资料:提单,箱单,发票准入门槛:须通过澳洲的TGA(治疗商品管理局)注册,符合标准规范:AS/NZS 1716:2012,此规范是澳大利亚和新西兰的呼吸保护装置标准。TGA(治疗商品管理局)是澳大利亚的治疗商品(包括药物、医疗器械、基因科技和血液制品)的监督机构。口罩要求:AS/NZS 1716:2012是澳大利亚和新西兰的呼吸保护装置标准,相关产品制造流程和测试必须符合本规范。
各国注册、认证简要办理流程
美国NIOSH认证
需按照NIOSH的指南实施,企业需寄送样品至NIOSH实验室实施测试,同时提交技术性资料(包括质量体系部分资料)至NIOSH文审,只有文审和测试都通过,NIOSH才核发批文。主要测试指标包括呼气阻力测试、呼气阀泄漏测试、吸气阻力测试、过滤效率测试。
美国FDA注册
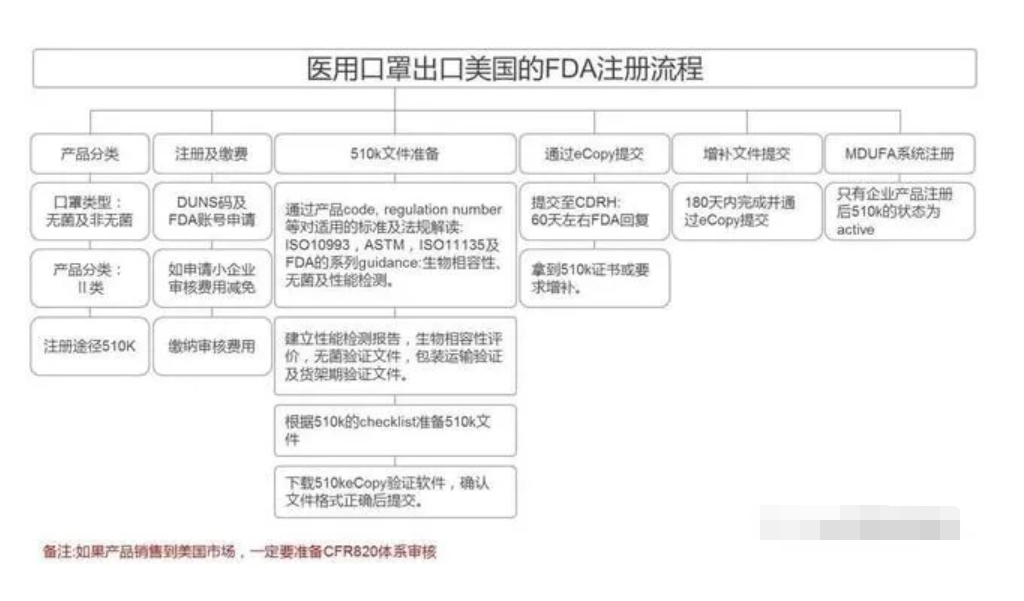
值得注意的是,对Ⅰ类产品,企业向FDA递交相关资料后,FDA只进行公告,并无相关证件发给企业。对Ⅱ、Ⅲ类器械,企业须递交PMN或PMA,FDA在公告的同时,会给企业以正式的市场准入批准函件(Clearance),即允许企业以自己的名义在美国医疗器械市场上直接销售其产品。
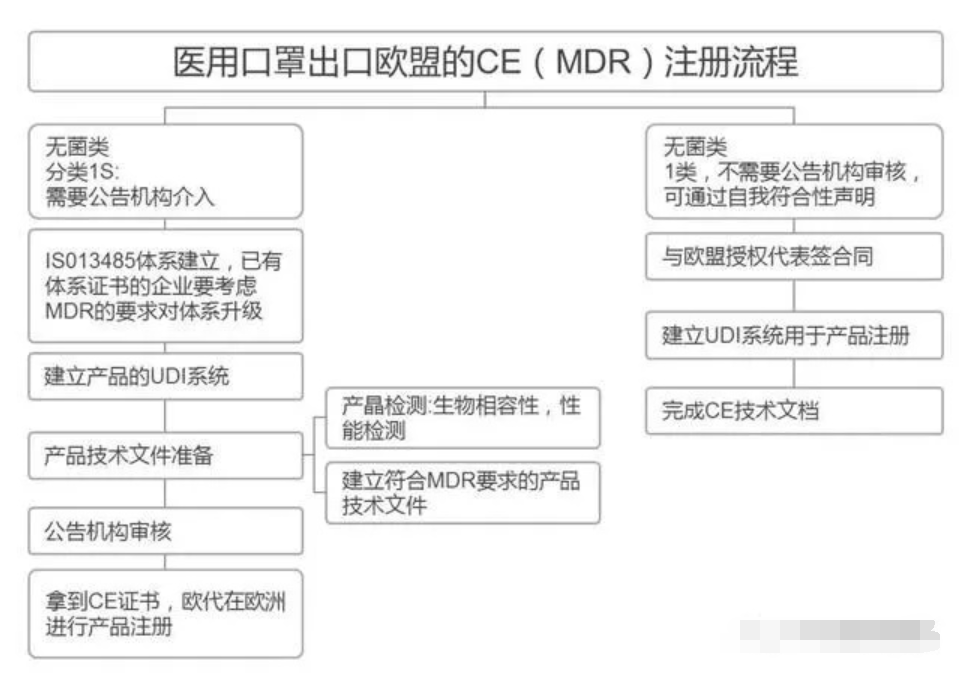
欧盟CE注册CE认证流程:① 认证申请——企业提供产品的技术资料,认证机构根据资料确定适用指令和标准;① 签署合同——企业和认证机构签署CE标志认证合同;② 产品预检——认证机构将样品送至授权的相关实验室测试;③ 产品终检——企业对产品进行调整,补齐相关手续,实验室给出最终检测报告;④ 企业整改——企业根据终检报告进行整改;⑤ 技术评审——实验室对产品进行技术评审;⑧ 证书签发——产品评审合格,由欧盟授权的公告机构给产品签发证书。
日本PMDA注册
1. 准备阶段。确定产品分类(I,II特殊控制,II类控制,III,IV)和产品JMDN编码,选择MAH(日本持证方);2. 制造商向PMDA注册工厂;3. II类特殊控制产品向授权认证机构PCB申请QMS工厂审核,其他II类产品和III类IV类产品向PMDA申请QMS工厂审核,并获得QMS证书;4. 申请Pre-Market Apporval证书,II类特殊控制由PCB发证,其他II类产品和III类IV类产品控制由MHLW(厚生劳动省)发证;5. 支付申请费用;6. 注册文件整改,注册批准;7. 所有类别产品均需要MAH向RBHW(厚生省地区机构)进行进口通报注册后才能进口销售。

韩国KFDA注册
韩国卫生福利部(MinistryofHealthandWelfare,MHW),简称卫生部,主要负责管食品、药品、化妆品和医疗器械的管理,是最主要的卫生保健部门。依照《医疗器械法》,韩国卫生福利部下属的食品药品安全部负责对医疗器械的监管工作。KFDA注册流程为:1. 确定产品分类(I,II,III,IV),选择KLH(韩国持证方);2. II类产品需申请KGMP证书和接受现场审核,II类产品一般是授权的第三方审核员,并获得KGMP证书;3. II类产品需要送样品到韩国MFDS授权的实验室进行韩国标准的测试;4. 由KLH向MFDS(韩国食品药品安全部)提交技术文件(检测报告,KGMP证书等),进行注册审批;5. 支付申请费用;6. 注册文件整改,注册批准;7. 指定韩国代理商和经销商,产品销售。
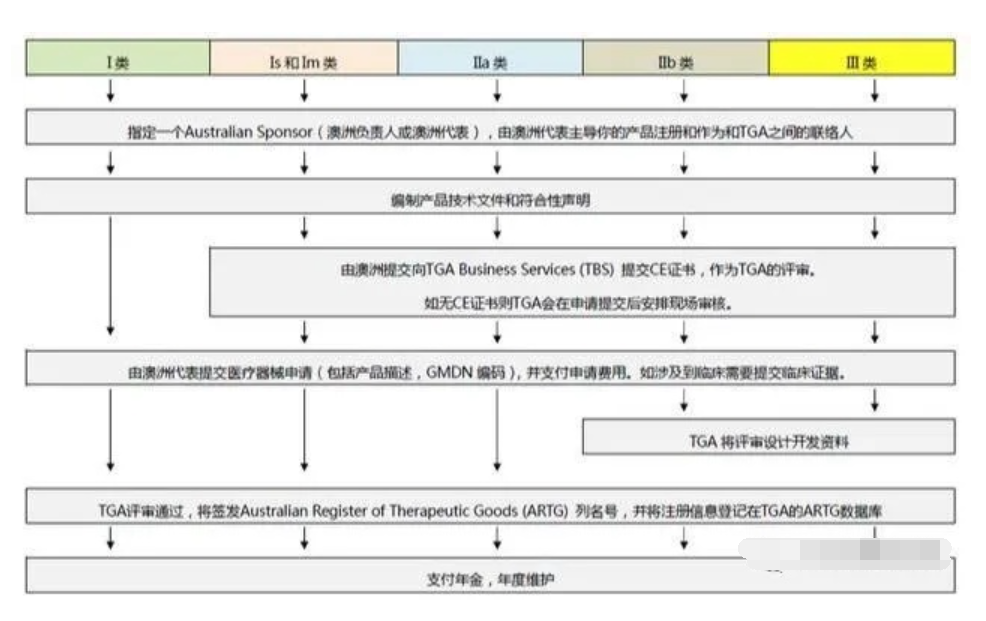
澳大利亚TGA注册
依据Australian Therapeutic Goods (Medical Devices) Regulations 2002,澳大利亚对医疗器械分为I类,Is and Im, IIa, IIb, III类,产品的分类几乎和欧盟分类一致,如产品已获得CE标志,则产品类别可以按照CE分类。值得注意的是,如已经获得欧盟公告机构(Notified Body)签发的CE证书,是可以被TGA认可的,并可以作为满足澳大利亚安全法规的重要注册资料。
更多关于防疫物资出口资讯,推荐您阅读:
﹥﹥什么是FDA认证?口罩出口美国需要FDA认证?一文告诉你
1.本站转载并注明其他来源的文章,均来自互联网或业内投稿人士,版权属于原版权人。转载请保留文章来源及作者,禁止擅自篡改,违者自负版权法律责任。
2.如发现本站文章存在版权问题,烦请提供版权疑问、版权证明、联系方式等发邮件至service@tuotuo-inc.com,我们将及时沟通与处理。
3.本站评论版块中各网友的评论只代表网友个人观点,不代表本站的观点或立场。





